Wie funktioniert eine Autobatterie und wie ist sie aufgebaut?
Dieser Beitrag ist wie folgt aufgeteilt:
Die Aufgabe der traditionell im Motorraum sitzenden Autobatterie ist allgemein bekannt: Ohne Batterie lässt sich das Fahrzeug nicht starten. Neben dem Anlasser brauchen auch Zündkerzen, Glühkerzen, Fahrzeugbeleuchtung und elektronische Assistenten elektrische Energie. Doch wie ist überhaupt der Aufbau einer Autobatterie und wie funktioniert sie?
Die Blei-Säure-Batterie: Bestandteile und Aufbau
Vielen Autofahrern und Autofahrerinnen ist vom Neukauf einer Batterie das hohe Gewicht einer Autobatterie bekannt – angefangen bei ca. 10.5 kg sind bis zu 30 kg möglich. Verantwortlich dafür sind die Bleiplatten in den Batteriezellen.
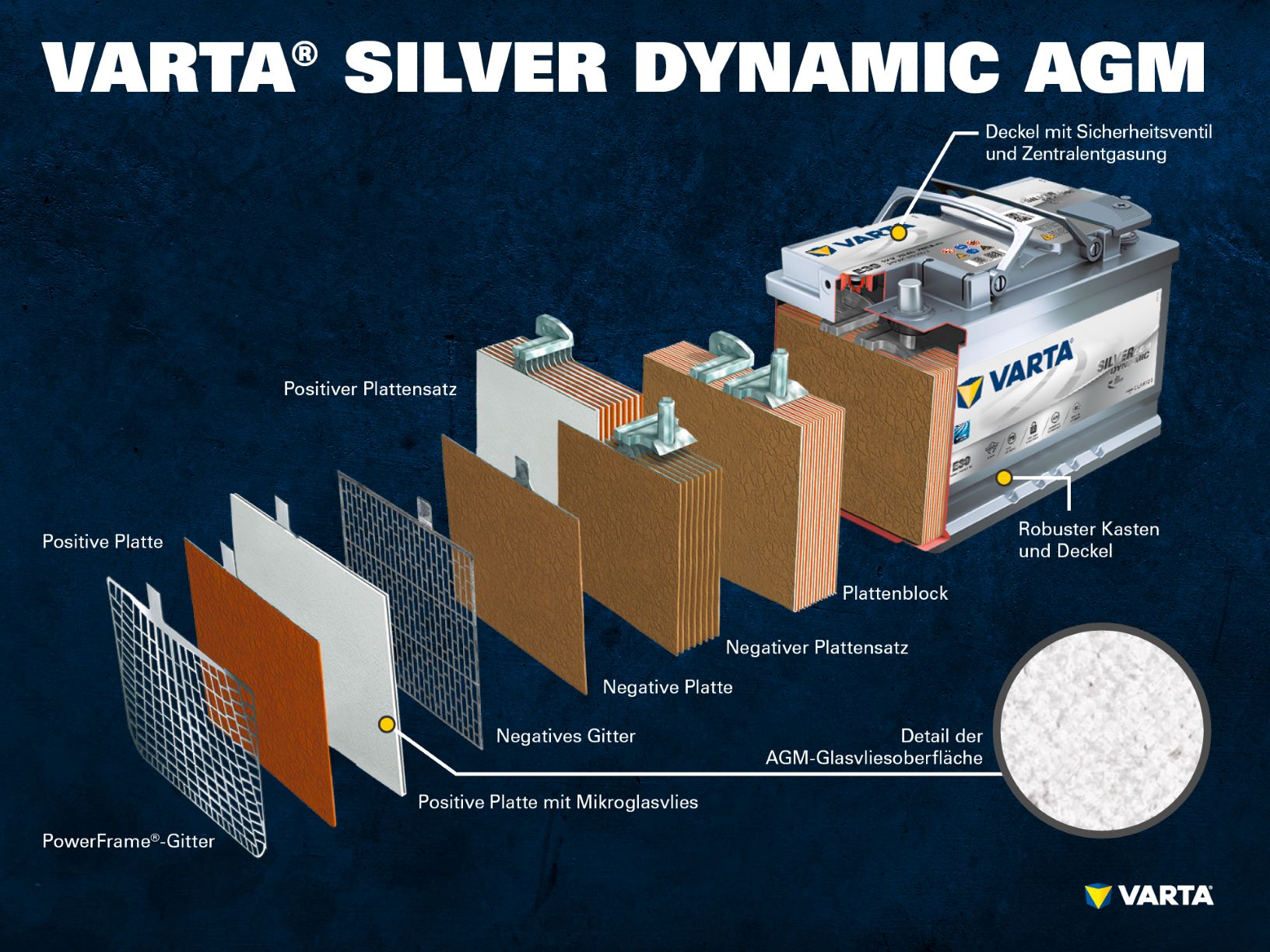
Bestandteile und Aufbau einer Batteriezelle
Positive Elektrode:
- Positive Platte: Die positiv geladene Platte (aktive Masse) besteht bei einer Blei-Säure-Batterie aus Bleioxid (PbO2) und ist in einen Elektrolyt getaucht.
- Positives Gitter: Die positive Gitter besteht aus einer Bleilegierung und dient zur Aufnahme der aktiven Masse und als Stromkollektor.
Negative Elektrode:
- Negative Platte: Die negativ geladene Platte (aktive Masse) besteht aus purem Blei (Pb) und ist ebenfalls in einen Elektrolyt getaucht.
- Negatives Gitter: Wie das positive Gitter besteht auch dieses aus einer Bleilegierung erfüllt denselben Zweck.
Getrennt werden die Elektroden unterschiedlicher Ladung durch eine Separatortasche.
Der Elektrolyt ist ein Gemisch aus Schwefelsäure und destilliertem Wasser (H2SO4). Dieser Elektrolyt kann flüssig (wie bei klassischen Nassbatterien oder der erweiterten EFB-Technologie), gelartig, oder in einem Glasvlies gebunden sein (wie bei der AGM-Technologie für erweiterte Start-Stopp-Anwendungen).
Mehrere positive Elektroden ergeben einen positiven Plattensatz und mehrere negative Elektroden ergeben einen negativen Plattensatz. Ein negativer und ein positiver Plattensatz zusammen ergeben einen Plattenblock. Ein Plattenblock ist eine Batteriezelle.

Eine konventionelle Starterbatterie besteht aus einer Reihenschaltung von 6 Zellen mit einer Nennspannung von jeweils rund 2 V und baut so im vollgeladenen Zustand eine Spannung von genau 12,72 V auf. Durch die Anzahl der Platten pro Zelle ergeben sich die Kapazität und die Kaltstartfähigkeit einer Batterie.
Faustregel: Desto mehr Platten sich in einer Zelle befinden, die somit zusammen eine größere Oberfläche bilden, desto mehr Kaltstartkraft (CCA) liefert eine Batterie. Wird der Raum der Zelle jedoch dafür genutzt weniger, aber dickere Platten unterzubringen, erhöht sich die Zyklenfestigkeit. Das heißt, die Batterie ist für einen höheren Ladungsdurchsatz (der stetige Auf- und Entladeprozess) konzipiert.
Die Zellen sind in einem Gehäuse aus einem säurefesten Plastik (Polypropylen) untergebracht. Dieses ist bei klassischen SLI-Batterien durch einen Deckel mit Labyrinthsystem geschlossen, welches das Auslaufen von Batterieflüssigkeit verhindert und die Flüssigkeit vom Gas trennt. Frühe Batterien hatten Schraubstopfen, welche das Nachfüllen von destilliertem Wasser ermöglichten. Heutige Batterien sind komplett wartungsfrei – es muss und darf kein Wasser nachgefüllt werden. Zwar haben auch AGM-Batterien noch „Einweg-Stopfen“, diese dürfen aber unter keinen Umständen geöffnet werden.
Funktion einer Autobatterie: Aus chemischer Energie wird elektrische Energie
Eine Autobatterie speichert Energie in chemischer Form und wandelt sie in elektrische Energie um. Bei diesem elektro-chemischen Prozess reagieren vier Materialien miteinander:
– Wasserstoff (H)
– Sauerstoff (O2)
– Blei (Pb)
– Schwefel (S)
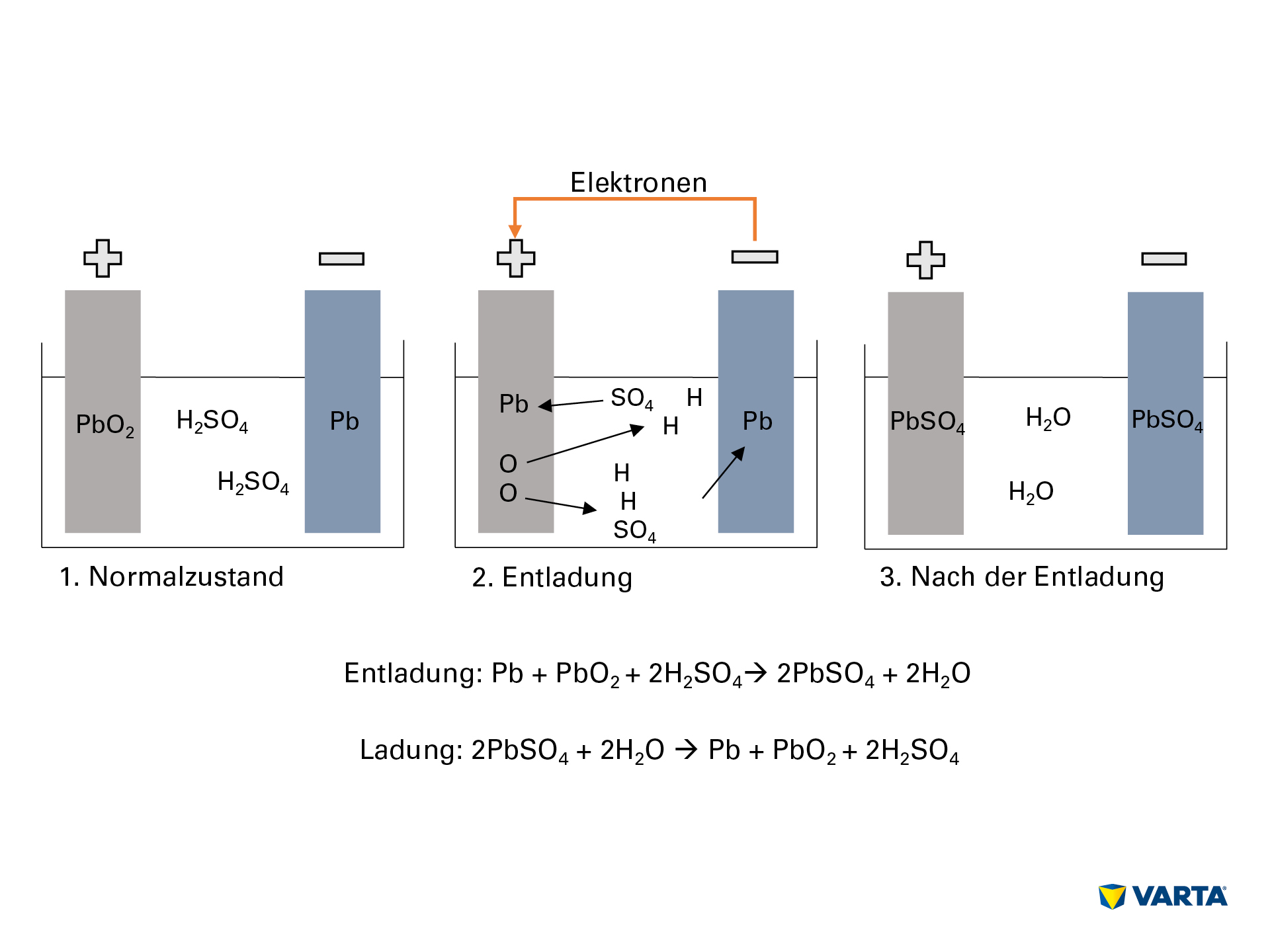
Durch das Anlegen eines externen Verbrauchers beginnt die chemische Reaktion in der Batterie:
- Der Elektrolyt, ein Gemisch aus Schwefelsäure und destilliertem Wasser (H2SO4), spaltet sich in positiv geladene Wasserstoffionen (H+) und negativ geladene Sulfationen (SO42-).
- Gleichzeitig wandern Elektronen (2e–) von der negativen zur positiven Elektrode über den externen Verbraucher.
- Um diesen Elektronenfluss auszugleichen, wandern Sulfationen vom Elektrolyt in die negative Elektrode und reagieren dort mit dem Blei (Pb), wodurch Bleisulfat (PbSO4) entsteht.
- Auch in der positiven Elektrode bildet sich Bleisulfat: Die Bindung des Sauerstoffs (O2) im Bleioxid (PbO2) wird durch die Elektronenwanderung gelöst und der Sauerstoff wandert in den Elektrolyt. Das zurückgebliebene Blei (Pb) bindet sich mit dem Sulfat (SO4) aus dem Elektrolyt.
- Dort bindet sich der Sauerstoff mit dem Wasserstoff zu Wasser (H2O). Da die Schwefelsäure durch die Bildung von Bleisulfat aufgebraucht wird, sinkt die Konzentration der Elektrolyt-Lösung. Sobald die Konzentration der Schwefelsäure auf ein bestimmtes Niveau fällt, muss die Batterie neu aufgeladen werden.
- Beim Aufladen laufen die chemischen Prozesse in umgekehrter Reihenfolge. Am Ende sind die ursprünglichen Elemente wiederzufinden: Die positive Elektrode besteht aus Bleisulfat (PbSO4), die negative Elektrode besteht aus purem Blei (Pb) und der Elektrolyt aus verdünnter Schwefelsäure (H2SO4).
Da dieser Wandlungsprozess verlustbehaftet ist, kann jede Autobatterie nur eine begrenzte Zahl von Zyklen überstehen. Ihre Nutzungsdauer ist daher begrenzt.
Probleme der Blei-Säure-Batterie: Sulfatierung und Säureschichtung
Wird eine Batterie mit einer zu geringen Spannung geladen oder läuft sie immer bei niedriger Spannung (unter 80%), entsteht Säureschichtung, auch Stratifikation genannt.
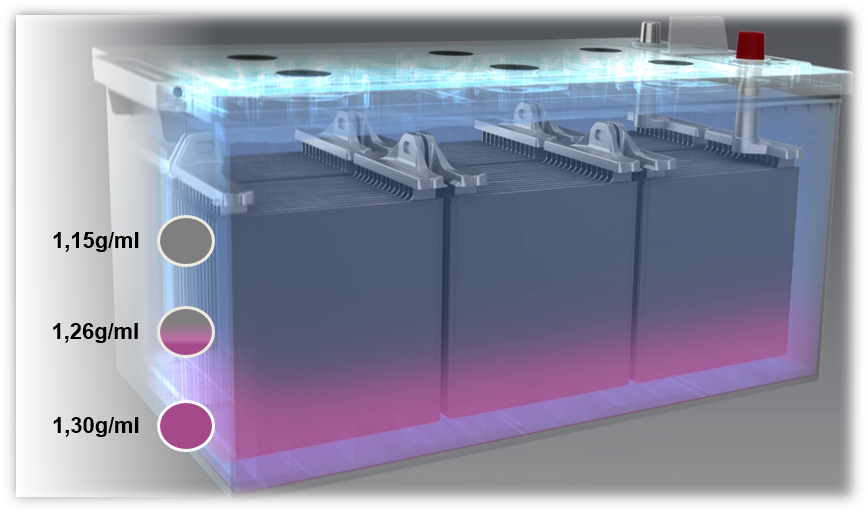
Dabei schichtet sich die Säure im Elektrolyt aufgrund einer mangelhaften Mischung dessen. Unterschiedliche Dichten verursachen die Schichtung von Schwefelsäure am Boden und Wasser im oberen Bereich der Batterie. Dadurch kann nur noch der mittlere Teil des Elektrolyt, also nur noch ein Drittel, für den Ent- und Aufladeprozess genutzt werden.
Eine mögliche Ursache für die Säureschichtung sind überwiegende Kurzstreckenfahrten bei gleichzeitiger Nutzung vieler elektrischer Verbraucher. Die Lichtmaschine hat in einem solchen Fall nicht genügend Zeit die Batterie genügend aufzuladen.
Eine Folge der Säureschichtung ist die Sulfatierung. Tritt diese in einer Batterie auf, oder wird sie konstant nicht ausreichend geladen, kristallisiert sich das Bleisulfat (PbSO4) an den Elektroden, aus denen über die Zeit größere Kristallgebilde entstehen. Dieser Vorgang wird „Sulfatierung“ genannt. Die Kristallisation verhindert die Rückwandlung von Bleisulfat in die ursprünglichen Komponenten Blei bzw. Bleioxid, was dazu führt, dass die Ladungsaufnahme gehemmt und die Kaltstartleitung verringert ist.Scharfe Kristalle können zudem die Separatoren beschädigen oder Zellkurzschlüsse verursachen.
Um diesen Effekten entgegenzuwirken und einen vorzeitigen Batterieausfall zu verhindern, sollte eine Batterie nie über eine längere Zeit einer Mangelladung ausgesetzt sein. Hierfür empfiehlt es sich, Batterien regelmäßig zu testen und bei Bedarf vollständig zu laden.
Sie wollen mehr zu diesem Thema erfahren? So wird eine Batterie richtig geladen.
Neue Batterietechnologien: AGM und Lithium-Ionen
Während konventionelle Blei-Säure-Batterien bislang noch einen hohen Anteil haben, ändert sich der Markt rasant: Innovative Batterietechnologien für Start-Stopp-Fahrzeuge wie die AGM verwenden in Vlies gebundene Säure für eine höhere Zyklenfestigkeit und garantieren in modernen Fahrzeugen mit erhöhtem Energiebedarf zuverlässige Leistung. Ein weiterer Vorteil der AGM: Eine Säureschichtung ist aufgrund der gebundenen Säure nicht mehr möglich.
Eine neue Generation von Autobatterien für Micro-Hybrid-Fahrzeuge arbeitet sogar mit 48 V und verwendet hierzu Zellen mit Lithium-Ionen-Technologie.