Jak działa akumulator samochodowy i jak jest zbudowany?
Spis treści
Tradycyjna funkcja akumulatora w pojeździe silnikowym jest powszechnie znana: bez akumulatora uruchomienie pojazdu jest niemożliwe. Poza rozrusznikiem, zasilania w energię elektryczną wymagają również świece zapłonowe, świece żarowe, oświetlenie oraz urządzenia elektroniczne. Jak skonstruowany jest akumulator i jak działa?
Akumulatory ołowiowo-kwasowe: podzespoły i budowa
Wielu kierowców dowiaduje się, ile waży akumulator dopiero przy jego zakupie. Akumulator samochodowy może ważyć od około 10,5 kg do 30 kg. Przyczyną tak dużej wagi są płyty ołowiowe w ogniwach akumulatora.
Elementy i budowa ogniwa akumulatora
Elektroda dodatnia:
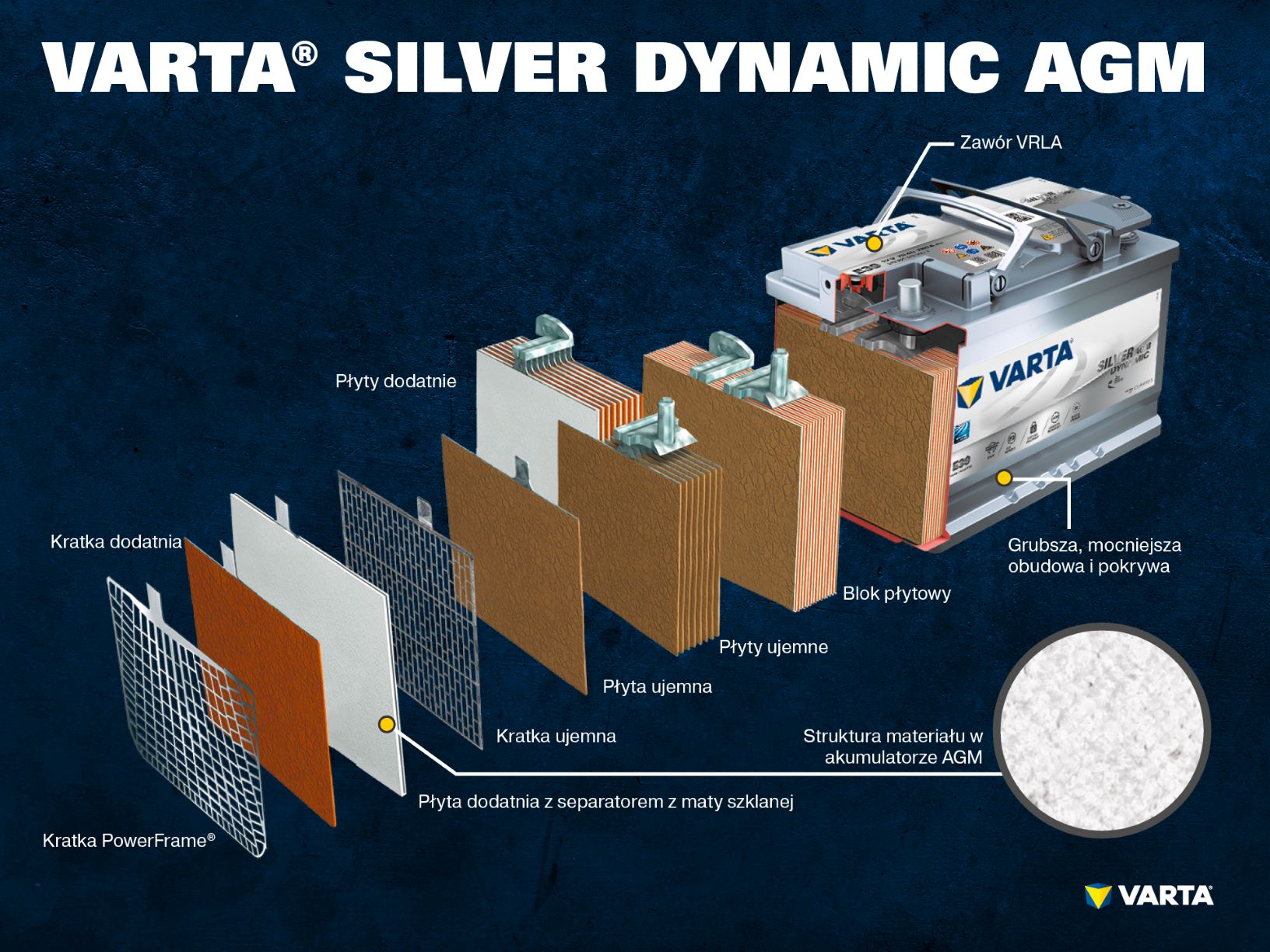
- Płyta dodatnia: W akumulatorze ołowiowo-kwasowym płyta z ładunkiem dodatnim (materiał aktywny) składa się z tlenku ołowiu (PbO2) zanurzonym w elektrolicie.
- Kratka dodatnia: Kratka dodatnia jest wykonana ze stopu ołowiu i służy do podtrzymywania materiału aktywnego oraz magazynowania prądu.
Elektroda ujemna:
- Płyta ujemna: Płyta z ładunkiem ujemnym (materiał aktywny) składa się z czystego ołowiu (Pb), który również jest zanurzony w elektrolicie.
- Kratka ujemna: Podobnie jak kratka dodatnia, również jest wykonana ze stopu ołowiu i służy do tego samego celu.
Elektrody z różnymi ładunkami są oddzielone separatorem.
Elektrolit to mieszanka kwasu siarkowego (H2SO4) i wody destylowanej. Elektrolit może mieć formę płynną (np. w tradycyjnych akumulatorach kwasowych (SLI) lub w akumulatorach z udoskonaloną technologią EFB), formę żelową lub może być zamknięty w szklanej macie (np. w technologii AGM, znajdującej zastosowanie w pojazdach z systemem start-stop).
Kilka elektrod dodatnich tworzy płytę dodatnią, a kilka elektrod ujemnych – ujemną. Płyta ujemna tworzy wraz z płytą dodatnią blok płytowy. Blok płytowy jest ogniwem akumulatora.
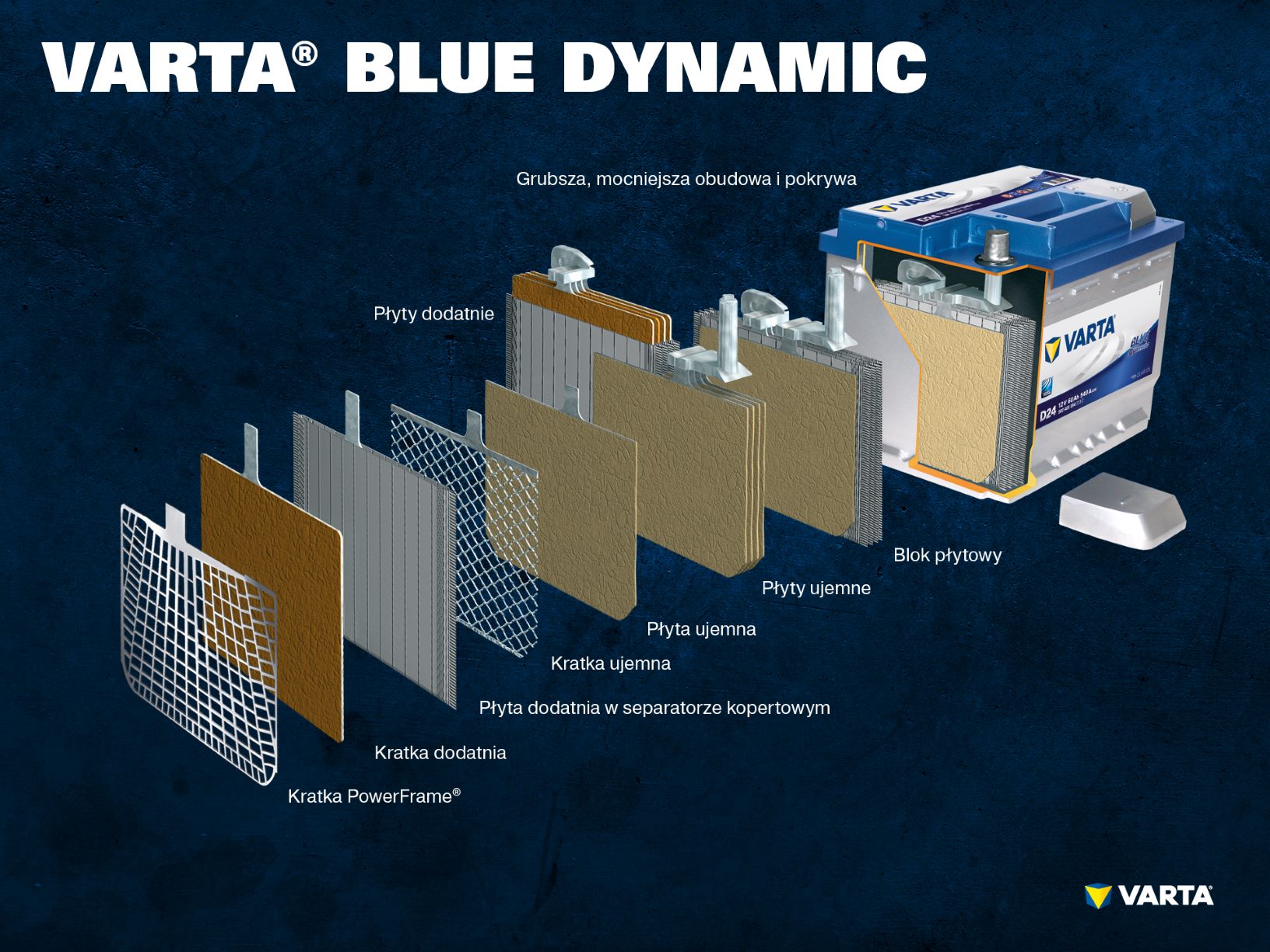
Tradycyjny akumulator rozruchowy składa się z 6 ogniw połączonych szeregowo, każdy o napięciu znamionowym 2,12 V, co daje w sumie napięcie 12,72 V przy pełnym naładowaniu akumulatora. Pojemność oraz moc rozruchu akumulatora zależy od liczby płyt w ogniwach.
Zasada: im więcej płyt w ogniwie, czyli im większą powierzchnię tworzą, tym większa moc rozruchu (CCA) zapewniana przez dany akumulator. Jeśli jednak dostępną przestrzeń w ogniwie zapełnimy mniejszą liczbą ale grubszych płyt, wówczas zwiększa się stabilność cyklu. To oznacza, że akumulator charakteryzuje się większą wydajnością cykliczną (proces ciągłego ładowania i rozładowywania).
Ogniwa są zamknięte w obudowie wykonanej z kwasoodpornego tworzywa sztucznego (polipropylenu). Tradycyjne akumulatory rozruchowe (SLI) są wyposażone w pokrywę z systemem labiryntu, który zapobiega wyciekaniu cieczy z akumulatora i oddziela ciecz od gazu.
Wcześniej w akumulatorach montowano odkręcane korki, dzięki którym można było dolewać do nich wody destylowanej. Nowoczesne akumulatory samochodowe są całkowicie bezobsługowe. Nie trzeba, a nawet nie można, dolewać do nich wody. Mimo że akumulatory AGM nadal mają „korki”, pod żadnym pozorem nie należy ich zdejmować.
Funkcje akumulatora samochodowego: energia chemiczna zostaje przekształcona w energię elektryczną
Akumulator samochodowy magazynuje energię w formie chemicznej i przekształca ją w energię elektryczną. W procesie elektrochemicznym cztery pierwiastki wchodzą ze sobą w reakcję:
- – Wodór (H)
- – Tlen (O2)
- – Ołów (Pb)
- – Siarka (S)
Podłączenie zewnętrznego odbiornika energii inicjuje reakcję chemiczną wewnątrz akumulatora:
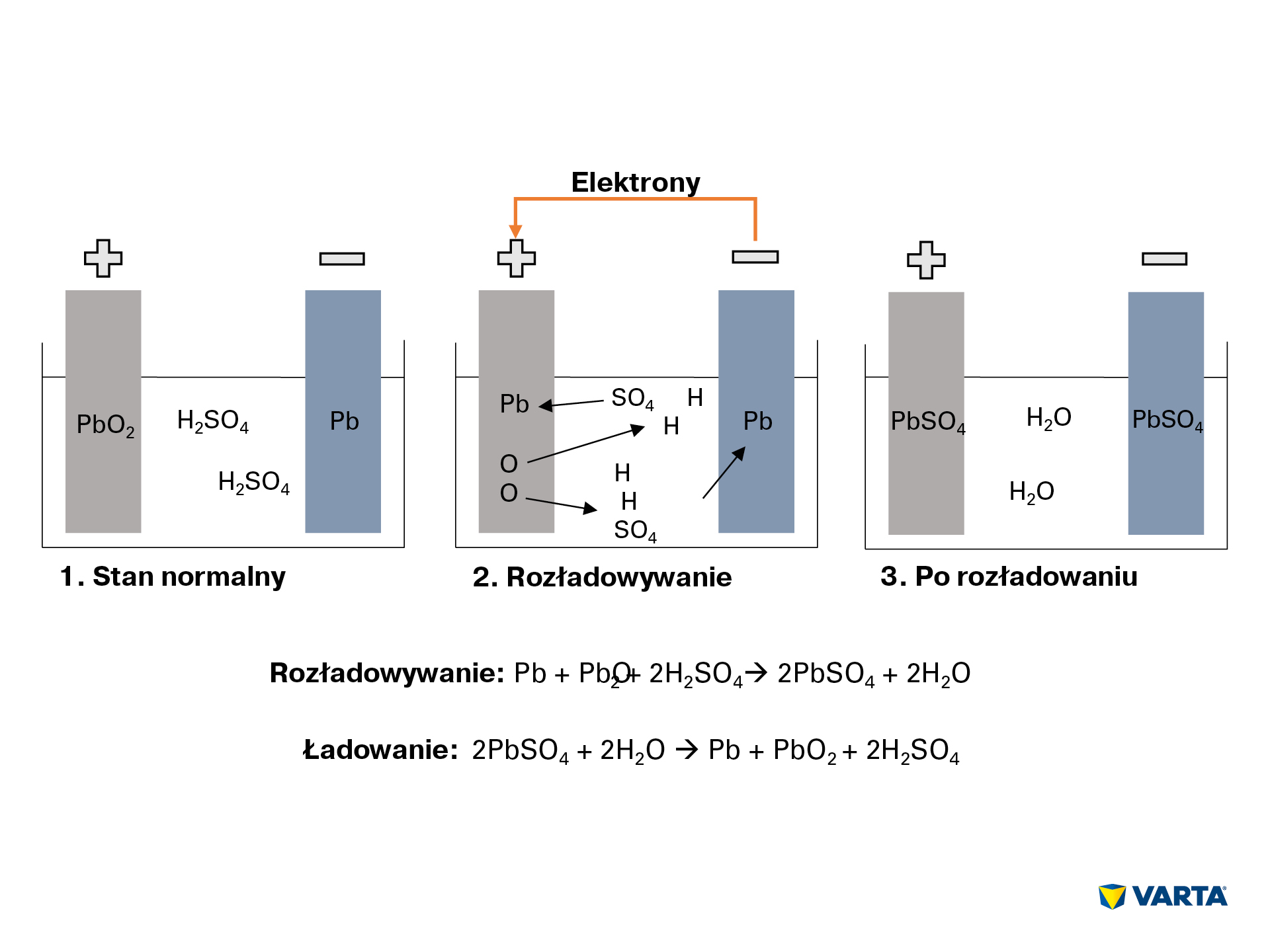
- elektrolit, czyli mieszanka kwasu siarkowego (H2SO4) i wody destylowanej, ulega rozpadowi na dodatnio naładowane jony wodoru (H+) i ujemnie naładowane jony siarczanowe (SO42-).
- Jednocześnie elektrony (2e–) przemieszczają się z elektrody ujemnej do elektrody dodatniej przez odbiornik zewnętrzny.
- Aby zrekompensować przepływ elektronów, jony siarczanowe przemieszczają się z elektrolitu do elektrody ujemnej, gdzie wchodzą w reakcję z ołowiem (Pb), w wyniku czego powstaje siarczan ołowiu (PbSO4).
- Siarczan ołowiu jest produkowany również w elektrodzie dodatniej: wiązanie tlenu (O2) w tlenku ołowiu (PbO2) zostaje rozerwane w wyniku transferu elektronów i tlen przechodzi do elektrolitu. Wówczas ołów (Pb) łączy się z siarczanem (SO4) z elektrolitu.
- Tam z kolei tlen łączy się z wodorem i powstaje woda (H2O). Ponieważ kwas siarkowy zostaje zużyty do utworzenia siarczanu ołowiu, stężenie roztworu elektrolitu spada. Gdy stężenie kwasu siarkowego spadnie poniżej określonego poziomu, akumulator wymaga ponownego naładowania.
- W trakcie ładowania procesy chemiczne odbywają się w odwróconej kolejności. Po zakończeniu całego procesu skład chemiczny wraca do pierwotnego stanu: elektroda dodatnia składa się z siarczanu ołowiu (PbSO4), elektroda ujemna z czystego ołowiu (Pb), a elektrolit z rozcieńczonego kwasu siarkowego (H2SO4). Ponieważ w wyniku tego odwróconego procesu generowane są straty, akumulator może obsłużyć ograniczoną liczbę cykli ładowania. Dlatego też jego żywotność jest ograniczona.
Problemy z akumulatorami ołowiowo-kwasowymi: zasiarczenie i rozwarstwienie elektrolitu
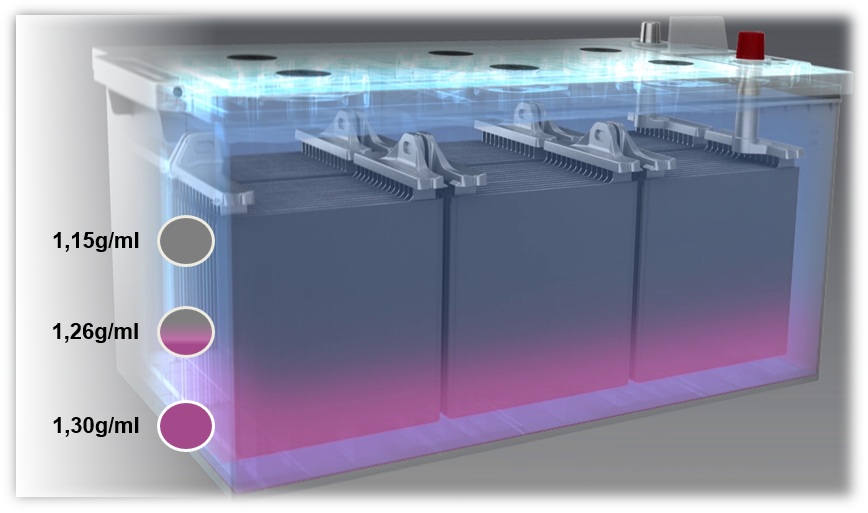
Jeśli akumulator zostanie naładowany prądem o zbyt niskim napięciu lub jeśli stale pracuje pod zbyt niskim napięciem (poniżej 80%), wówczas dochodzi do zjawiska nazywanego rozwarstwieniem kwasu, nazywanego też stratyfikacją. Kwas w elektrolicie ulega stratyfikacji ze względu na słabe wymieszanie. Różnice w gęstości powodują osiadanie kwasu siarkowego na dnie i wypychanie wody do górnej części akumulatora. Z tego powodu wyłącznie środkowa część elektrolitu, czyli tylko jedna trzecia, może zostać wykorzystana w procesie rozładowywania i ładowania.
Możliwą przyczyną takiego stanu rzeczy są głównie krótkie podróże przy korzystaniu z dużej liczby odbiorników elektrycznych w samochodzie. Wówczas alternator nie ma wystarczającej ilości czasu na doładowanie akumulatora.
Skutkiem rozwarstwienia kwasu w akumulatorze jest jego zasiarczenie. Jeśli to zjawisko wystąpi lub jeśli akumulator nie będzie stale ładowany do wystarczającego poziomu, wówczas siarczan ołowiu (PbSO4) ulega krystalizacji na elektrodach, po pewnym czasie tworząc większe struktury kryształów. Ten proces nazywa się „zasiarczeniem”. Krystalizacja uniemożliwia ponowne przekształcenie siarczanu ołowiu w ołów czy tlenek ołowiu, co skutkuje brakiem możliwości przyjmowania ładunku i zmniejszeniem mocy zimnego rozruchu.
Ostre kryształy mogą ponadto uszkodzić separatory lub powodować zwarcia w ogniwach.
Aby przeciwdziałać temu zjawisku i zapobiegać przedwczesnemu zużyciu akumulatora, nie należy narażać go na niski poziom naładowania przez dłuższy czas. Dlatego zalecane jest regularne testowanie akumulatora i jego pełne ładowanie w razie potrzeby.
Czy chcesz dowiedzieć się więcej na ten temat? Jak prawidłowo ładować akumulator.
Nowe technologie akumulatorów: akumulatory AGM i litowo-jonowe
Do niedawna tradycyjne akumulatory kwasowo-ołowiowe miały spory udział w rynku. Jednakże rynek szybko się zmienia: W innowacyjnych technologiach akumulatorów do pojazdów z systemem start-stop, takich jak akumulatory AGM, wykorzystywane są nasączone kwasem maty, które zapewniają większą stabilność cyklu oraz gwarantują niezawodność w pojazdach o zwiększonym poborze energii. Kolejna zaleta technologii AGM: dzięki uwięzieniu elektrolitu w macie zjawisko rozwarstwiania kwasu nie występuje.
Nowa generacja akumulatorów samochodowych do mikro hybryd działa pod napięciem 48 V i wykorzystuje ogniwa wykonane w technologii litowo-jonowej.